Како батерије раде и раде
 У најширем смислу те речи у технологији, термин "батерија" се односи на уређај који омогућава под одређеним условима рада да се акумулира одређена врста енергије, ау другим да се користи за људске потребе.
У најширем смислу те речи у технологији, термин "батерија" се односи на уређај који омогућава под одређеним условима рада да се акумулира одређена врста енергије, ау другим да се користи за људске потребе.
Користе се тамо где је потребно прикупити енергију за одређено време, а затим је користити за обављање великих радно интензивних процеса. На пример, хидраулички акумулатори који се користе у преводницама омогућавају бродовима да се уздигну на нови ниво на кориту реке.
Електричне батерије раде са струјом по истом принципу: прво акумулирају (акумулирају) електричну енергију из спољашњег извора пуњења, а затим је дају прикљученим потрошачима да раде. По својој природи спадају у хемијске изворе струје који су способни да изводе периодичне циклусе пражњења и пуњења више пута.
Током рада, хемијске реакције се стално одвијају између компоненти електродних плоча са њиховом супстанцом за пуњење - електролитом.
Шематски дијаграм батеријског уређаја може се представити поједностављеним цртежом када су две плоче од различитих метала са жицама уметнуте у тело посуде како би се обезбедили електрични контакти. Између плоча се сипа електролит.
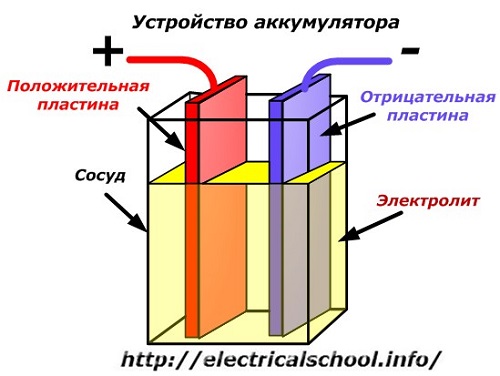
Рад батерије када је празна
Када се оптерећење, као што је сијалица, повеже са електродама, ствара се затворено електрично коло кроз које протиче струја пражњења. Настаје кретањем електрона у металним деловима и ањона са катјонима у електролиту.
Овај процес је конвенционално приказан на дијаграму са дизајном никл-кадмијум електроде.
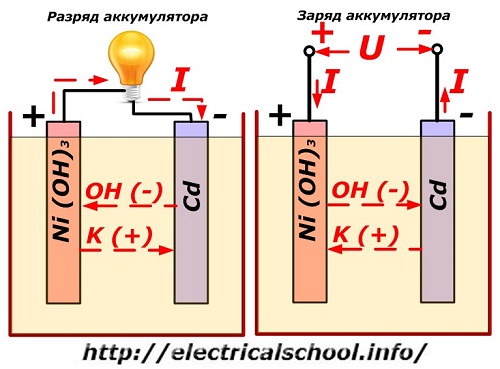
Овде се као материјал позитивне електроде користе оксиди никла са графитним адитивима, који повећавају електричну проводљивост. Метал негативне електроде је сунђераст кадмијум.
Током пражњења, честице активног кисеоника из никл оксида се ослобађају у електролит и усмеравају на негативне плоче, где се кадмијум оксидује.
Перформансе батерије при пуњењу
Када је оптерећење искључено, на терминале плоче се примењује константан (у одређеним ситуацијама пулсирајући) напон веће вредности од напуњене батерије истог поларитета, када се плус и минус терминали извора и потрошача поклапају. .
Пуњач увек има више снаге, што „потискује“ заосталу енергију у батерији и ствара електричну струју у смеру супротном од пражњења. Као резултат тога, унутрашњи хемијски процеси између електрода и електролита се мењају. На пример, на кутији никл-кадмијумских плоча, позитивна електрода је обогаћена кисеоником, а негативна - до стања чистог кадмијума.
Када се батерија испразни и напуни, хемијски састав материјала плоча (електрода) се мења, али се електролит не мења.
Методе повезивања батерије
Паралелна веза
Количина струје пражњења коју особа може да издржи зависи од многих фактора, али пре свега од дизајна, коришћених материјала и њихових димензија. Што је већа површина плоча на електродама, то је већа струја коју могу издржати.
Овај принцип се користи за паралелно повезивање ћелија истог типа у батеријама када је потребно повећати струју до оптерећења.Али за пуњење таквог дизајна биће потребно повећати снагу извора. Ова метода се ретко користи за готове структуре, јер је сада много лакше одмах купити потребну батерију. Али произвођачи киселих батерија га користе, повезујући различите плоче у појединачне блокове.
Серијска веза
У зависности од материјала који се користи, може се створити напон од 1,2 / 1,5 или 2,0 волти између две електродне плоче батерија уобичајених у свакодневном животу. (Заправо, овај опсег је много шири.) Очигледно, није довољан за многе електричне уређаје. Дакле, батерије истог типа су повезане у серију, а то се често ради у једном случају.
Пример таквог дизајна је широко распрострањени развој аутомобила заснован на сумпорној киселини и плочама са оловним електродама.
Обично, међу људима, посебно међу возачима транспорта, уобичајено је да се сваки уређај назове батеријом, без обзира на број његових саставних елемената - кутије. Међутим, ово није сасвим тачно.Конструкција, састављена од неколико кутија повезаних у низу, већ је батерија, за коју је стављен скраћени назив «АКБ»... Њена унутрашња структура је приказана на слици.
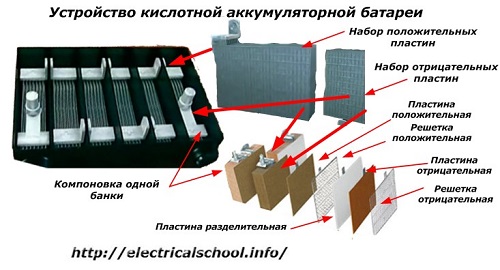
Свака од тегли се састоји од два блока са сетом плоча за позитивне и негативне електроде. Блокови се уклапају један у други без металног контакта са могућношћу поуздане галванске везе преко електролита.
У овом случају, контактне плоче имају додатну решетку и одвојене су једна од друге сепаратором.
Повезивање плоча у блокове повећава њихову радну површину, смањује укупни отпор целе структуре и омогућава вам да повећате снагу прикљученог оптерећења.
На спољној страни кутије, таква батерија има елементе приказане на слици испод.
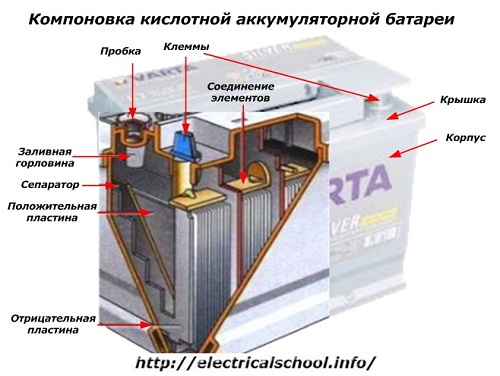
Показује да је чврсто пластично кућиште запечаћено поклопцем и опремљено са два терминала (обично у облику конуса) на врху за повезивање са електричним колом аутомобила. Ознаке поларитета су утиснуте на њиховим терминалима: «+» и «-». Обично позитивни терминал има нешто већи пречник од негативног терминала да блокира грешке у ожичењу.
Поправљиве батерије имају отвор за пуњење на врху сваке посуде за контролу нивоа електролита или додавање дестиловане воде током рада. У њега је уврнут утикач који штити унутрашње шупљине кућишта од контаминације и истовремено спречава изливање електролита када се батерија нагне.
Пошто је са снажним пуњењем могуће гасирање из електролита (а овај процес је могућ током интензивне вожње), у чеповима се праве рупе како би се спречило повећање притиска унутар кутије.Кроз њих излазе кисеоник и водоник, као и паре електролита. Препоручује се избегавање таквих ситуација које укључују прекомерне струје пуњења.
На истој слици је приказана веза елемената између обала и распоред плоча електрода.
Стартер акумулатори за аутомобиле (оловне киселине) раде на принципу двоструке сулфатизације. Током пражњења / пуњења на њима се одвија електрохемијски процес, праћен променом хемијског састава активне масе електрода са ослобађањем / апсорпцијом воде у електролиту (сумпорна киселина).
Ово објашњава повећање специфичне тежине електролита при пуњењу и смањење када се батерија испразни. Другим речима, вредност густине вам омогућава да процените електрично стање батерије. За његово мерење користи се посебан уређај - ауто хидрометар.
Дестилована вода, која је део електролита киселих батерија, на негативним температурама прелази у чврсто стање - лед.Због тога, како би се спречило смрзавање акумулатора аутомобила по хладном времену, потребно је применити посебне мере предвиђене правилима за експлоатацију.
Које врсте батерија постоје?
Савремена производња за различите намене производи више од три десетине производа са различитим саставом електрода и електролита. 12 познатих модела ради само на литијуму.

Следеће се може наћи као метал електроде:
-
олово;
-
гвожђе;
-
литијум;
-
титанијум;
-
кобалт;
-
кадмијум;
-
никл;
-
цинк;
-
сребро;
-
ванадијум;
-
алуминијум
-
неке друге ствари.
Они утичу на електричне излазне карактеристике, а самим тим и на примену.
Способност да издрже краткорочна велика оптерећења која произилазе из ротације радилице мотора са унутрашњим сагоревањем помоћу електростартера карактеристична је за оловно-киселинске батерије. Широко се користе у транспорту, беспрекидним изворима напајања и системима за хитно напајање.
Стандард галванске ћелије (обичне батерије) обично се замењују никл-кадмијумским, никл-цинк и никл-метал хидридним батеријама.
Али литијум-јонски или литијум-полимерни дизајни поуздано функционишу у мобилним и рачунарским уређајима, грађевинским алатима, па чак и електричним возилима.
Према врсти коришћеног електролита, батерије су:
-
кисело
-
алкалне.
Постоји класификација батерија према намени. На пример, у савременим условима појавили су се уређаји који се користе за пренос енергије — пуњење других извора. Такозвана екстерна батерија помаже власницима многих мобилних уређаја у одсуству наизменичне електричне мреже. У стању је да више пута пуни таблет, паметни телефон, мобилни телефон.
Све ове батерије имају исти принцип рада и сличан уређај. На пример, литијум-јонски модел прстију приказан на слици испод на много начина понавља дизајн киселинских батерија о којем је раније било речи.
Овде видимо исте контактне електроде, плоче, сепаратор и кућиште. Само они су направљени узимајући у обзир друге услове рада.
Основне електричне карактеристике батерије
На рад уређаја утичу параметри:
-
капацитет;
-
густина енергије;
-
самопражњење;
-
температурни режим.
Капацитет се назива максимално пуњење батерије, које је у стању да да током пражњења до најнижег напона. Изражава се у привесцима (СИ систем) и ампер-часовима (несистемска јединица).
Као врста капацитета постоји „енергетски капацитет“, који одређује енергију која се ослобађа током пражњења до минимално дозвољеног напона. Мери се у џулима (СИ) и ват-сатима (не-СИ јединице).
Густина енергије изражена као однос количине енергије према тежини или запремини батерије.
Самопражњење узима у обзир губитак капацитета након пуњења у одсуству оптерећења на терминалима. Ово зависи од дизајна и погоршава се кваровима изолације између електрода из много разлога.
Радна температура утиче на електрична својства и у случају озбиљних одступања од норме коју је навео произвођач, може оштетити батерију. Топлота и хладноћа су неприхватљиви, утичу на ток хемијских реакција и притисак околине унутар кутије.
